|
KCSG 연구 논문 소개 |
|
|
■ KCSG GU11-05
Cancer Res Treat. 2018 Oct;50(4):1252-1259. Phase II Study of Dovitinib in Patients with Castration-Resistant Prostate Cancer (KCSG-GU11-05)  Q. 연구의 배경은? 거세저항성 전립선암의 경우, 최근 수많은 항암신약들의 개발에도 불구하고 치료 전략이 상당히제한적입니다. 특히, 연구를 계획하였던 2011년 당시에는 더욱 새로운 치료가 절실하였습니다. 전립선암의 암 발생 과정과 전이 과정에 Fibroblast growth factor (FGF) 신호전달체계가 중요하다고 알려져 있고, dovotinib은 vascular endothelial growth factor receptor (VEGFR), platelet-derived growth factor receptor와 fibroblast growth factor receptor (FGFR)에 결합하는multitargeted receptor tyrosine kinase inhibitor로서, 특히 FGF pathway을 타 약제보다 잘 억제한다고 알려져 있습니다. Q. 연구의 목적은? 본 연구에서는 전이성 거세저항성 전립선암 환자에서, dovitinib의 항암효과를 확인하고자 하였습니다. Q. 연구 방법? 본 연구는 2상 다기관 연구로 2012년부터 2015년까지 모집된 거세저항성 전립선암 환자 44명을 대상으로 하였습니다. 등록된 환자는 dovitinib 500mg을 5일 복용 후 2일 휴약하였습니다. 16주 무진행생존율을 1차 유효성 평가변수로 두었고, 그 외에 전체생존기간, 독성, PSA 반응율을 조사하고, VEGFR2, FGF23, FGFR2 등의 바이오마커 연구도 함께 진행하였습니다. Q. 연구 결과? 11개의 기관에서 44명의 환자가 등록되었습니다. 이 중 80%의 환자는 docetaxel 투여 경험이 있는 환자였고, 82%에서는 골전이, 23%에서는 간전이를 동반하였습니다. 16주 무진행생존율은 42.1%였고, 무진행 생존기간은 3.67개월, 전체 생존기간은 13.7개월이었습니다. 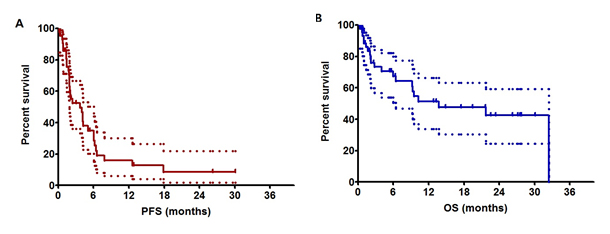 그림 1. 무진행생존기간 (A), 전체생존기간 (B). 점선은 95% 신뢰구간
그림 1. 무진행생존기간 (A), 전체생존기간 (B). 점선은 95% 신뢰구간
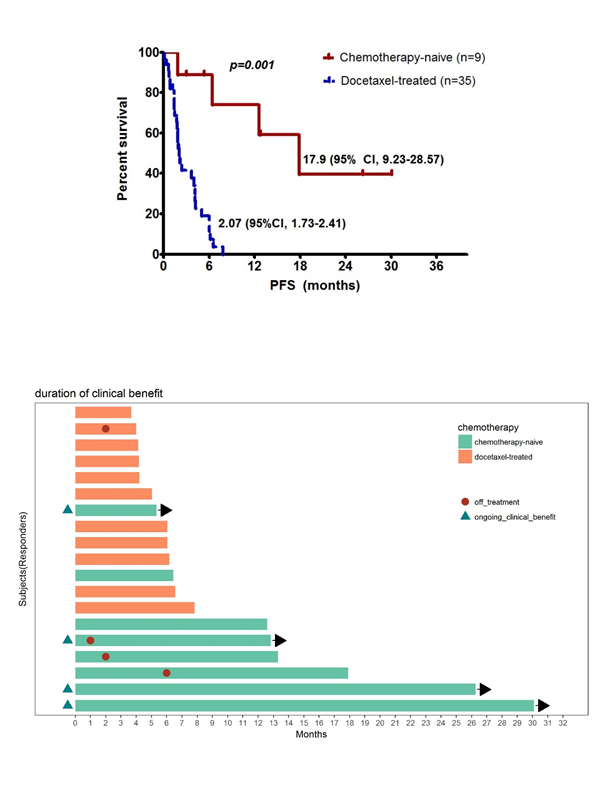
Biomarker 연구로 시행되었던 치료 전후 FGFR2, VEGFR2, FGF-23 농도의 변화는 뚜렷하지 않았고, 유일하게 치료 전 VEGFR2 농도가 높은 환자에서 무진행생존기간이 연장되는 것을 확인하였습니다. Q. 마지막으로 하고 싶은 말은? Dovitinib 약제 개발이 중단되어 아쉽고, 항암치료 전후의 FGF signaling의 변화나 predictive biomarker 등의 개발 등의 숙제가 남아 있습니다만, 항암치료 전 거세저항성 전립선암 환자에 있어서 FGF signaling 차단의 가능성을 확인할 수 있었던 계기라고 판단합니다. 물론, 풍족하지 못한 상황에서 KCSG GU/GY 분과의 도움으로 연구 설계, 참여 기관 모집을 원활하게 진행할 수 있었고, 물심양면 환자를 등록해 주신 11개 기관의 연구자 선생님들과 연구코디네이터 선생님들, 그리고 도와주신 KCSG 데이터센터 선생님들께 감사한 마음을 전합니다. 제1저자 최윤지 (고려대학교 안암병원) 
■ KCSG LU12-13 Cancer Res Treat. 2019 Apr;51(2):718-726 A Randomized, Open-Label, Phase II Study Comparing Pemetrexed Plus Cisplatin Followed by Maintenance Pemetrexed versus Pemetrexed Alone in Patients with Epidermal Growth Factor Receptor (EGFR)-Mutant Non-small Cell Lung Cancer after Failure of First-Line EGFR Tyrosine Kinase Inhibitor: KCSG-LU12-13  Q. 연구의 배경은?
EGFR 돌연변이를 가진 진행성 비소세포폐암 환자에서 1차 요법으로 EGFR-TKI 를 사용한 이후에 질병이 진행했을 경우 NCCN guideline 은 cytotoxic chemotherapy 로 pemetrexed (Alimta®) 와 platinum 의 병합 요법을 추천하고 있으나 현재 국내 요양 급여 기준에 따라서는 pemetrexed 를 단독 요법으로만 사용할 수 있습니다.
Q. 연구의 배경은?
EGFR 돌연변이를 가진 진행성 비소세포폐암 환자에서 1차 요법으로 EGFR-TKI 를 사용한 이후에 질병이 진행했을 경우 NCCN guideline 은 cytotoxic chemotherapy 로 pemetrexed (Alimta®) 와 platinum 의 병합 요법을 추천하고 있으나 현재 국내 요양 급여 기준에 따라서는 pemetrexed 를 단독 요법으로만 사용할 수 있습니다.2015년 Lung Cancer 지에 발표된 후향연구(Lee, Sun et al. 2015)에서는 pemetrexed/platinum 병합요법이 pemetrexed 단독요법보다 우월한 질병조절율과 무진행생존기간의 향상을 보여준 바가 있습니다. Q. 연구의 목적은? 국내에서는 EGFR-TKI 1차 요법에 실패한 비소세포폐암 환자들에게 pemetrexed 를 단독 요법으로 밖에 사용할 수가 없는데, 앞서 말씀드린 후향 연구의 결과에 따라 pemetrexed/platinum 병합 요법이 pemetrexed 단독 요법보다 더 우월함을 확인하기 위해 디자인된 연구입니다. 또한 이 연구는 보건복지부 암정복과제 중 공익적 사업을 위한 과제로 선정이 되어 대한항암요법연구회(KCSG)에서 다기관연구로 진행되었습니다. Q. 연구 방법? 본 연구는 다기관 제 2상 연구로 EGFR-TKI 1차 요법에 실패한 EGFR 돌연변이 비소세포폐암 환자들이 pemetrexed/platinum 병합 요법군(실험군, PC군)과 pemetrexed 단독 요법군(대조군, P군)에 1:1 로 무작위 배정되었습니다. 환자들은 질병의 진행이 확인될 때까지 6주기의 pemetrexed/platinum 병합치료 후 pemetrexed 단독치료를 받거나(PC군) 처음부터 pemetrexed 단독치료를 받았습니다(P군). 연구의 1차 목적은 무진행생존기간(PFS)이었으며, 2차 목적으로 전체반응률(ORR), 전체생존기간(OS), 삶의 질 평가(HRQoL)와 치료에 따른 이상반응을 평가하였습니다. Q. 연구 결과? 이 연구에는 국내 14개 기관에서 96명의 환자들이 등록되었으며, 91명의 환자(PC군 46명 vs. P군 45명)를 분석하였습니다. 전체반응률(ORR)은 PC군 34.8%(16/46)와 P군 17.8%(8/45)으로 차이를 보였으나 통계학적인 유의성은 없었습니다.(p=0.066) 1차 목적인 무진행생존기간(PFS) PC군 5.4개월, P군 6.4개월이었으며(p=.114), 전체생존기간(OS)은 PC군 17.9개월, P군 15.7개월로 차이를 보이지 않았습니다.(P=.787) 삶의 질과 이상반응에서도 양 군간에 유의한 차이는 없었습니다. 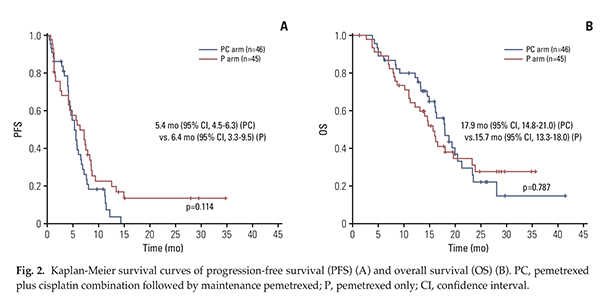
이 연구는 대한항암요법연구회(KCSG)를 통해 국내의 많은 기관이 참여한 다기관연구로 진행되었습니다. 지면을 빌어 연구에 참여해 주신 여러 기관의 연구자 선생님께 다시 한번 감사의 말씀을 올립니다. 제1저자 유쾌한 (가천대학교 길병원) 
■ KCSG GU11-03 Cancer Res Treat. 2019 Oct;51(4):1578-1588. Temsirolimus in Asian Metastatic/Recurrent Non-clear Cell Renal Carcinoma  Q. 연구의 배경은?
전체 신포암의 8-20%를 차지하고 있는 비 투명세포암(non-clear cell type)은 조직학적으로 다양하며 전반적으로 투명세포암(clear cell type) 보다 예후가 불량합니다. Global Advanced Renal Cell Cancer (ARCC) 에서 진행한 3상 연구에서 Temsirolimus라는 mTOR 억제제가 투명 및 비 투명세포암에서 효과가 있음을 밝혀졌으며 이후로 예후가 불량한 비 투명세포암에서 1차 치료제로 승인을 받았습니다. 본 연구는 KCSG를 통한 다기관, 제2상, 이전에 치료 받지 않은 비 투명 신세포암 환자들을 대상으로 temsirolimus의 효과를 알아보기 위한 연구 입니다.
Q. 연구의 목적은?
본 연구에서 일차 목표는 이전에 치료 받지 않은 비투명 신세포암 환자들을 대상으로 temsirolimus 치료의 무진행 생존기간을 알아 보고자 하였습니다. 이차 목표로는 전체 생존기간, 종양반응률과, 질병통제율과 약제의 부작용을 알아보고자 하였습니다.
Q. 연구 방법?
본 연구는 총 44명의 비투명 신세포암 환자들을 대상으로 ARCC에서 제시한 예후과 무관하게 Temsiroliums의 효과를 알아보고자 하였습니다. KCSG를 통해 전향적으로 10명의 환자들을 등록 및 모집 중에 예후가 불량한 비 투명세포암에서 Temsirolimus가 1차 약제로 승인을 받으면서 본 연구는 조기 중단되었습니다. 따라서 후향적으로 34명의 환자들을 추가로 모집하여 연구를 진행하였습니다.
Q. 연구 결과?
본 연구에서 비투명 신세포암 환자들의 가장 흔한 조직학적 특성은 papillary type (24명, 54%)였으며 이외에도 chromophobe (11명, 25%), collecting duct (2명, 5%), Xp11.2 translocation (1명, 2%) 등이 있었습니다. Temsirolimus를 1차 약제로 투여한 비투명 신세포암 환자들의 무진행 생존기간 (median progression free survival)은 7.6 개월이었고, 중앙 전체 생존기간 (median overall survival, OS)은 17.6개월이었습니다. 종양반응률 (overall response rate, ORR)은 11% 였으며 질병통제율(clinical benefit rate, CBR)은 83%였습니다. 이전에 신장절제술 시행한 환자들은 더 긴 무진행 생존기간 (HR 0.16; 95% confidence interval [CI], 0.06 to 0.42; p<0.001)과 전체 생존기간(HR, 0.15; 95% CI, 0.05 to 0.45; p<0.001)을 보였습니다.
Q. 연구의 배경은?
전체 신포암의 8-20%를 차지하고 있는 비 투명세포암(non-clear cell type)은 조직학적으로 다양하며 전반적으로 투명세포암(clear cell type) 보다 예후가 불량합니다. Global Advanced Renal Cell Cancer (ARCC) 에서 진행한 3상 연구에서 Temsirolimus라는 mTOR 억제제가 투명 및 비 투명세포암에서 효과가 있음을 밝혀졌으며 이후로 예후가 불량한 비 투명세포암에서 1차 치료제로 승인을 받았습니다. 본 연구는 KCSG를 통한 다기관, 제2상, 이전에 치료 받지 않은 비 투명 신세포암 환자들을 대상으로 temsirolimus의 효과를 알아보기 위한 연구 입니다.
Q. 연구의 목적은?
본 연구에서 일차 목표는 이전에 치료 받지 않은 비투명 신세포암 환자들을 대상으로 temsirolimus 치료의 무진행 생존기간을 알아 보고자 하였습니다. 이차 목표로는 전체 생존기간, 종양반응률과, 질병통제율과 약제의 부작용을 알아보고자 하였습니다.
Q. 연구 방법?
본 연구는 총 44명의 비투명 신세포암 환자들을 대상으로 ARCC에서 제시한 예후과 무관하게 Temsiroliums의 효과를 알아보고자 하였습니다. KCSG를 통해 전향적으로 10명의 환자들을 등록 및 모집 중에 예후가 불량한 비 투명세포암에서 Temsirolimus가 1차 약제로 승인을 받으면서 본 연구는 조기 중단되었습니다. 따라서 후향적으로 34명의 환자들을 추가로 모집하여 연구를 진행하였습니다.
Q. 연구 결과?
본 연구에서 비투명 신세포암 환자들의 가장 흔한 조직학적 특성은 papillary type (24명, 54%)였으며 이외에도 chromophobe (11명, 25%), collecting duct (2명, 5%), Xp11.2 translocation (1명, 2%) 등이 있었습니다. Temsirolimus를 1차 약제로 투여한 비투명 신세포암 환자들의 무진행 생존기간 (median progression free survival)은 7.6 개월이었고, 중앙 전체 생존기간 (median overall survival, OS)은 17.6개월이었습니다. 종양반응률 (overall response rate, ORR)은 11% 였으며 질병통제율(clinical benefit rate, CBR)은 83%였습니다. 이전에 신장절제술 시행한 환자들은 더 긴 무진행 생존기간 (HR 0.16; 95% confidence interval [CI], 0.06 to 0.42; p<0.001)과 전체 생존기간(HR, 0.15; 95% CI, 0.05 to 0.45; p<0.001)을 보였습니다.
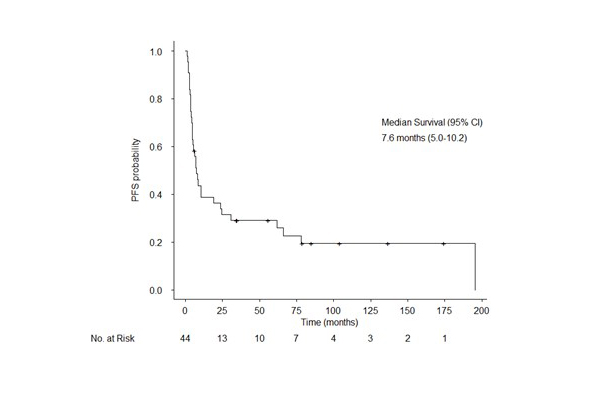 Figure 1. Progression-free survival (PFS) of temsirolimus in nccRCC
Figure 1. Progression-free survival (PFS) of temsirolimus in nccRCC
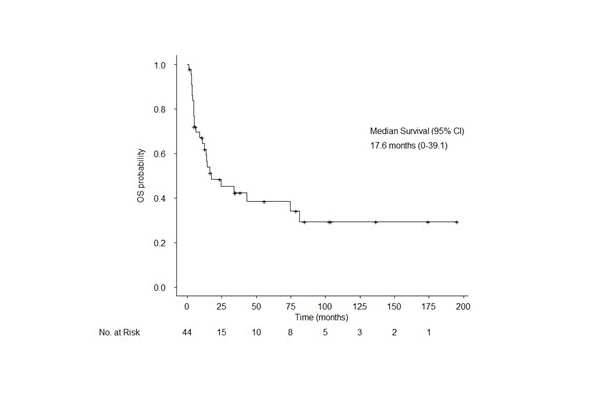 Figure 2. Overall survival (OS) of temsirolimus in nccRCC
Figure 2. Overall survival (OS) of temsirolimus in nccRCC
비 투명세포 신세포암은 흔하지 않은 암종이며 다양한 조직학적 특성을 가지고 있어 연구하기 어려운 암종이지만 여러 기관의 선생님들의 도움으로 환자들을 등록하여 연구를 진행할 수 있었습니다. 데이터 분석 및 논문을 완성하는 과정까지 도움을 주신 모든 선생님들께 감사드립니다. 제 1저자 이기쁨 (연세의료원) 
■ KCSG PC13-09 J Geriatr Oncol. 2019 Sep;10(5):749-756 Serum biomarkers for predicting overall survival and early mortality in older patients with metastatic solid tumors  Q. 연구의 배경은? 한국 사회의 고령화와 더불어 암을 진단받는 환자들의 연령분포도 점차 고령화가 되고 있습니다. 진료실에서는 다양한 노인 암환자를 만나게 되지만 그 안에는 건강한 노인 암환자가 있는 반면 노쇠하여 세포독성 항암제와 같은 치료를 견디지 못하는 노인 암환자가 뒤섞여 있습니다. 이러한 노인 암환자들을 기능적인 노화에 따라서 구분해내는 것은 임상의들에게 큰 숙제였습니다. 때마침 국내에서 노인 암환자의 항암치료 전 노인포괄평가(Comprehensive Geriatric Assessment)를 시행하여 항암독성을 예측하는 다기관 연구가 분당서울대병원 김지현 교수님의 주도로 KCSG에서 진행되었습니다(KCSG PC13-09). 그러나, 노인포괄평가의 경우 검사 항목들이 매우 다양하고 복잡하여 한국의 진료현실에서 적용하기 어려운 면이 있었고, 혈액에서 노화를 대변할 수 있는 마커가 있다면 진료에 활용할 수 있겠다는 생각을 하게 되었습니다. Q. 연구의 목적은? 노인 암환자의 혈액을 채취하여 그 안에서 확인할 수 있는 항목 중 기능적인 노화를 대변할 수 있는 바이오마커를 찾아내어 예후와 연관되는지를 탐색하는 것이었습니다. Q. 연구 방법? 본 연구는 모 연구인 KCSG PC13-09 연구에 참여한 70세 이상의 4기 노인 고형암환자 301명 중에서 항암치료 시작 전 혈액샘플에 동의한 138명의 환자들의 혈청을 분석하였습니다. 분석 전에는 문헌고찰을 통해서 노화에 따른 생체기능의 저하와 관련되었다고 보고된 마커들을 찾아보았고 13가지 혈액마커를 선정하였습니다. 혈액마커의 분석에는 ELISA와 Luminex multiplex assay를 이용하였습니다. 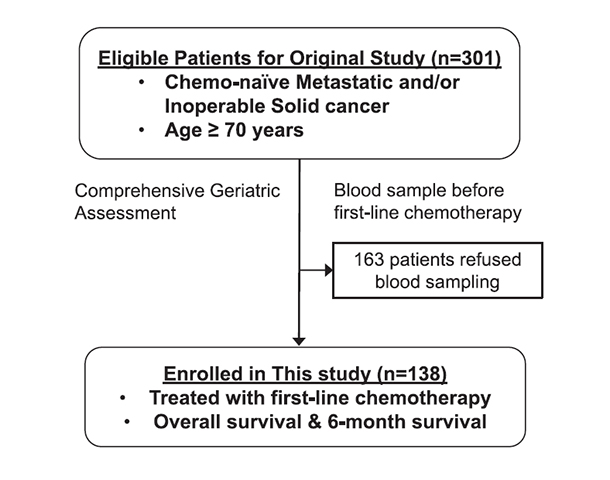 그림 1. 연구의 모식도
그림 1. 연구의 모식도
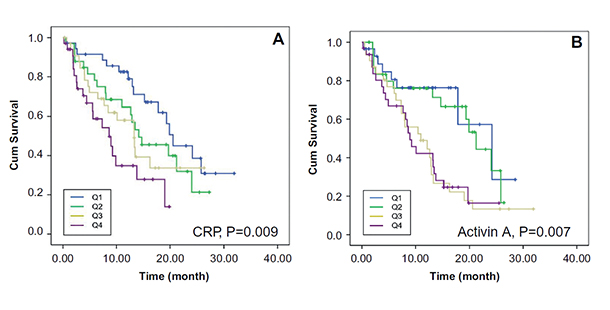 그림 2. CRP와 Activin A의 혈청농도에 따른 노인 암환자의 카플란마이어 생존곡선
그림 2. CRP와 Activin A의 혈청농도에 따른 노인 암환자의 카플란마이어 생존곡선
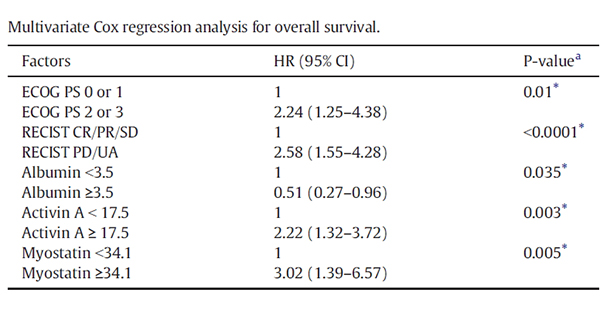 표 1. 노인 암환자의 전체생존기간에 대한 Cox 회귀분석
표 1. 노인 암환자의 전체생존기간에 대한 Cox 회귀분석

■ KCSG PC17-01 Cancer Res Treat. 2019;51(4):1632-1638 Feasibility Study of Physician Orders for Life-Sustaining Treatment for Patients with Terminal Cancer  Q. 연구의 배경은?
2009년 세브란스 김할머니 사건을 계기로 무의미한 연명의료의 중단에 대한 사회적 관심이 높아지게 되었고 각계각층의 치열한 논의 끝에 ‘호스피스·완화의료 및 임종과정에 있는 환자의 연명의료 결정에 관한 법률’ (약칭: 연명의료결정법)이 제정되어 2018년 2월부터 말기 및 임종기 환자의 진료과정에 적용되고있습니다. 말기 혹은 임종기 환자는 임종 시 연명의료를 원하는 지에 대해 스스로 결정할 수 있으며 이를 의료진이 연명의료계획서 (Physician Orders of Life-Sustaining Treatment, POLST)의 형태로 작성, 보관하게 됩니다. 이 과정을 통해 환자의 자기결정권을 존중하고 나아가 임종기 삶의 질의 개선을 기대할 수 있습니다. 그러나 국내에서는 이를 진료현장에 적용하기에는 아직 많은 장애물들이 있습니다. 특히 나쁜 소식은 되도록 환자에게 직접 알리지 않고 가족들과 의료진 사이에 논의 및 결정되어왔으며, 연명의료에 대한 논의가 사망직전에 이루어지는 경우가 많아 환자는 임종기 의사결정과정에서 배제되는 경우가 일반적이었습니다. 그 외에 죽음에 대한 논의를 터부시 하는 문화, 제도에 대한 지식의 부족이나 과정의 복잡성 등도 장애요인이 될 수 있습니다.
Q. 연구의 목적은?
본 연구는 말기 암 환자를 대상으로 진료 일선에서 연명의료계획서의 적용 가능성을 확인하고 장애요인을 분석하여 가능한 해결책을 제시하고자 하며, 나아가 연명의료결정법의 안정적 정착을 준비하고자 계획되었습니다.
Q. 연구의 배경은?
2009년 세브란스 김할머니 사건을 계기로 무의미한 연명의료의 중단에 대한 사회적 관심이 높아지게 되었고 각계각층의 치열한 논의 끝에 ‘호스피스·완화의료 및 임종과정에 있는 환자의 연명의료 결정에 관한 법률’ (약칭: 연명의료결정법)이 제정되어 2018년 2월부터 말기 및 임종기 환자의 진료과정에 적용되고있습니다. 말기 혹은 임종기 환자는 임종 시 연명의료를 원하는 지에 대해 스스로 결정할 수 있으며 이를 의료진이 연명의료계획서 (Physician Orders of Life-Sustaining Treatment, POLST)의 형태로 작성, 보관하게 됩니다. 이 과정을 통해 환자의 자기결정권을 존중하고 나아가 임종기 삶의 질의 개선을 기대할 수 있습니다. 그러나 국내에서는 이를 진료현장에 적용하기에는 아직 많은 장애물들이 있습니다. 특히 나쁜 소식은 되도록 환자에게 직접 알리지 않고 가족들과 의료진 사이에 논의 및 결정되어왔으며, 연명의료에 대한 논의가 사망직전에 이루어지는 경우가 많아 환자는 임종기 의사결정과정에서 배제되는 경우가 일반적이었습니다. 그 외에 죽음에 대한 논의를 터부시 하는 문화, 제도에 대한 지식의 부족이나 과정의 복잡성 등도 장애요인이 될 수 있습니다.
Q. 연구의 목적은?
본 연구는 말기 암 환자를 대상으로 진료 일선에서 연명의료계획서의 적용 가능성을 확인하고 장애요인을 분석하여 가능한 해결책을 제시하고자 하며, 나아가 연명의료결정법의 안정적 정착을 준비하고자 계획되었습니다.1차 목적: 연명의료계획서 작성율 (연명의료계획서 작성/전체 말기 암환자) 2차 목적: 연명의료계획서 작성의 장애요인 조사 Q. 연구 방법? 7개 기관 (가천대학교 길병원, 가톨릭대학교 부천성모병원, 성빈센트병원, 서울특별시 서울의료원, 영남대학교병원, 울산대학교병원, 한림대학교 동탄성심병원) 이 참여하였으며 혈액종양내과에 방문한 환자 중 말기 암으로 진단된 20세 이상의 환자를 대상으로 하였습니다. 말기암의 정의는 대한의학회의 말기 및 임종기 판단 지침에 따라 다음 항목 중 1개 이상에 해당하는 경우 말기환자로 정의하였습니다. 1) 적극적인 암치료에도 불구하고 암으로 인하여 수개월 이내에 사망할 것으로 예상되는 상태, 2) 암의 진행으로 인하여 일상생활의 수행 능력이 심각히 저하되고 신체 장기의 기능이 악화되어 회복을 기대하기 어려운 상태. 단 의식이 저하되고 있거나 의사소통이 어려운 환자는 본 연구의 대상에서 제외하였습니다. 연구 절차는 외래 및 입원 환자 중 위의 선정/ 제외 기준에 맞는 말기암 환자에게 연명의료계획서에 대한 간단한 설명과 함께 안내문을 제공하였습니다. 이후 원하는 시기에 논의한 뒤 최종적으로 작성이 완료된 경우 연명의료작성을 하였다고 정의하였습니다. 이 과정에서 의사가 안내를 하지 못한 경우는 의사에게 ‘의사의 장애요인’ 에 대한 설문지를 작성하도록 하였으며, 환자가 안내를 받았으나 논의를 거부하거나 최종 작성까지 가지 못한 경우 환자에게 ‘환자의 장애요인’ 에 대한 설문지를 작성하도록 하였습니다. Q. 연구 결과? 2017년 6월부터 12월까지 총 336명의 환자가 등록되었습니다. 60.4%의 환자가 ECOG 3/ 4로 수행능력이 불량하였으며, 41.2%는 호스피스 돌봄을 받고 있었습니다. 37.8%는 항암치료 후 병이 진행한 환자였으나 현재 항암치료를 받고 있거나 (15.8%), 암을 막 진단받은 환자 (5.1%) 도 포함되었습니다. 의사의 판단에 따른 예측여명은 10.6±7.3주 였습니다 (표1). 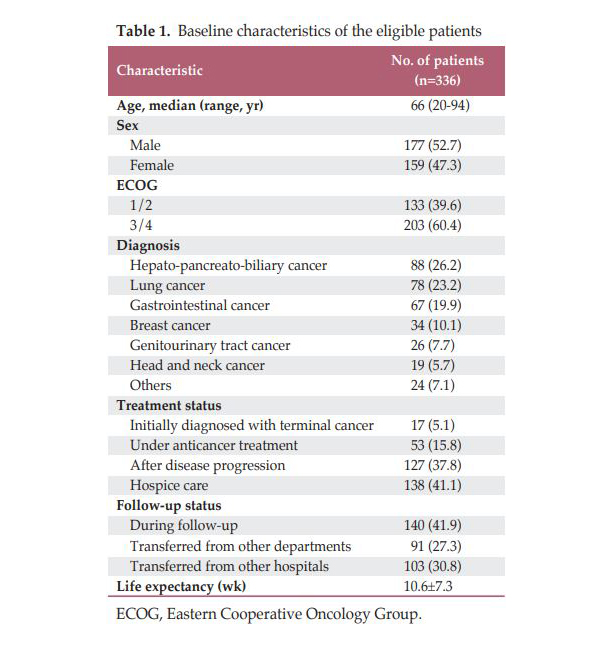
의사의 입장에서 연명의료계획서를 작성하기 어려운 장애요인으로는 가족이 환자에게 이야기를 하는것을 원치 않거나 의견차이가 있는 경우 (49.7%), 의사가 나쁜 소식을 환자에게 직접 전하기 꺼려하는 경우 (44.8%) 가 주를 이루었으며, 환자에게 희망을 빼앗거나 포기로 비춰질것 같은 죄책감 (21.5%), 환자가 본인의 병 상태나 예후에 대해 알기를 거부하거나 회피하는 경우 (34.3%), 예후를 예측하기 어려운 경우 (21.0%), 또는 적절한 논의의 시기를 찾기 어려운 경우 (16.6%) 로 조사되었습니다 (표2). 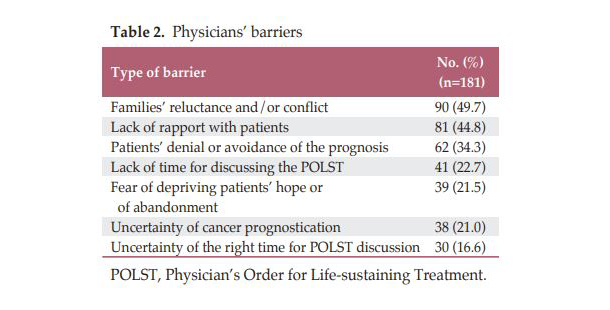
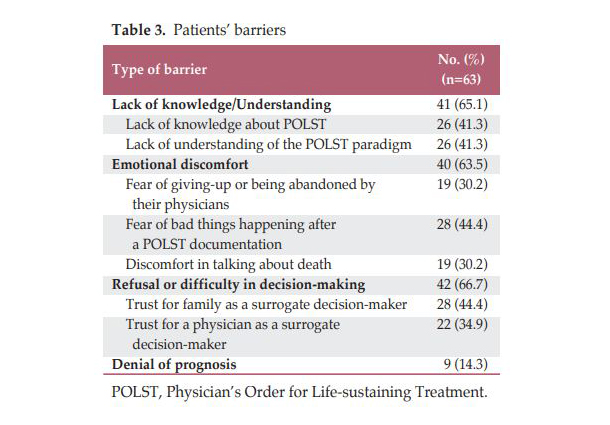

■ KCSG BR11-06 Br J Cancer. 2019 Dec;121(12):985-990. Randomised Phase 2 study of lapatinib and vinorelbine vs vinorelbine in patients with HER2 + metastatic breast cancer after lapatinib and trastuzumab treatment (KCSG BR11-16).  Q. 연구의 배경은?
최근 HER2양성 전이성 유방암 치료에 많은 새로운 약제가 도입되면서 치료결과의 많은 향상을 가져 왔습니다. 그러나 대부분의 경우 질병의 진행을 경험하게 되고, 후속 치료를 어떻게 구성할지는 여전히 중요한 문제입니다. 전이성 HER2양성 유방암의 초기 항암약제의 실패 후 치료원칙은, 항HER2 제제를 유지하면서, 기본토대가 되는 세포독성항암제를 변경하는 것입니다. Lapatinib 은 trastuzumab 의 치료 실패 후 사용되는 대표적인 항HER2 제제입니다. 본 연구는 HER2 양성 유방암의 치료에 있어서, trastuzumab 및 lapatinib을 포함하는 항HER2 치료제의 실패 후, lapatinib 을 포함한 항암치료를 지속하는 것이 효과적인지 살펴보기 위하여 시행하였습니다.
Q. 연구의 목적은?
전이성 HER2 양성 유방암에서 초기 trastuzumab 및 lapatinib 을 포함한 항암요법에 실패 후 lapatinib 과 vinorelbine 의 병합요법이 효과적인지 평가하고자 하였습니다.
Q. 연구 방법?
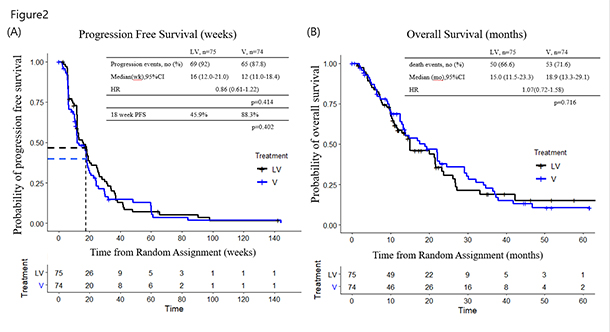
대상환자는 Lapatinib 을 포함한 최소 2가지 이상의 항HER2 제제를 사용 후, 질병의 진행을 경험했어야 하며, Lapatinib 사용시 PR/CR 또는 최소 12주 이상 SD 반응을 보였어야 했습니다. 환자는 vinorelbine 및 lapatinib 병합 군 (LV) 과 vinorelbine 단독군(V)으로 1:1 무작위 배정이 되었습니다. 1차 목표는 18주 시점에서 무진행생존(PFS)이었고, 2차 목표는 반응율(ORR), 무진행생존(PFS) 및 전체 생존(OS)이었습니다.
Q. 연구 결과?
Lapatinib 및 vinorelbine 병합군이 vinorelbine 단독군에 비하여, 18주 시점의 PFS에서 유의한 차이를 보여주지 못하였습니다. (45.9 % vs 38.9 % , p=0.402) 객관적 반응율(ORR)은 19.6% 대 16.9%로 (p=0.881) 역시 차이가 없었으며, 전체 PFS 및 OS 도 양 군간에 큰 차이를 보여주지 못하였습니다.
Q. 연구의 배경은?
최근 HER2양성 전이성 유방암 치료에 많은 새로운 약제가 도입되면서 치료결과의 많은 향상을 가져 왔습니다. 그러나 대부분의 경우 질병의 진행을 경험하게 되고, 후속 치료를 어떻게 구성할지는 여전히 중요한 문제입니다. 전이성 HER2양성 유방암의 초기 항암약제의 실패 후 치료원칙은, 항HER2 제제를 유지하면서, 기본토대가 되는 세포독성항암제를 변경하는 것입니다. Lapatinib 은 trastuzumab 의 치료 실패 후 사용되는 대표적인 항HER2 제제입니다. 본 연구는 HER2 양성 유방암의 치료에 있어서, trastuzumab 및 lapatinib을 포함하는 항HER2 치료제의 실패 후, lapatinib 을 포함한 항암치료를 지속하는 것이 효과적인지 살펴보기 위하여 시행하였습니다.
Q. 연구의 목적은?
전이성 HER2 양성 유방암에서 초기 trastuzumab 및 lapatinib 을 포함한 항암요법에 실패 후 lapatinib 과 vinorelbine 의 병합요법이 효과적인지 평가하고자 하였습니다.
Q. 연구 방법?
대상환자는 Lapatinib 을 포함한 최소 2가지 이상의 항HER2 제제를 사용 후, 질병의 진행을 경험했어야 하며, Lapatinib 사용시 PR/CR 또는 최소 12주 이상 SD 반응을 보였어야 했습니다. 환자는 vinorelbine 및 lapatinib 병합 군 (LV) 과 vinorelbine 단독군(V)으로 1:1 무작위 배정이 되었습니다. 1차 목표는 18주 시점에서 무진행생존(PFS)이었고, 2차 목표는 반응율(ORR), 무진행생존(PFS) 및 전체 생존(OS)이었습니다.
Q. 연구 결과?
Lapatinib 및 vinorelbine 병합군이 vinorelbine 단독군에 비하여, 18주 시점의 PFS에서 유의한 차이를 보여주지 못하였습니다. (45.9 % vs 38.9 % , p=0.402) 객관적 반응율(ORR)은 19.6% 대 16.9%로 (p=0.881) 역시 차이가 없었으며, 전체 PFS 및 OS 도 양 군간에 큰 차이를 보여주지 못하였습니다.

■ KCSG GU10-16 European Journal of Cancer 2020 Mar;127:183-190 Gemcitabine plus carboplatin versus gemcitabine plus oxaliplatin in cisplatin-unfit patients with advanced urothelial carcinoma: a randomised phase II study (COACH, KCSG GU10-16)  Q. 연구의 배경은?
진행성 요로상피세포암 (urothelial cancer)의 일차 표준요법은 백금기반 항암제이며, 백금제제 중에서도 cisplatin을 기반으로 하는 복합항암제가 추천됩니다. 백금제제에는 여러 약제가 있지만, cisplatin이 특별히 추천되는 이유는 cisplatin과 carboplatin을 비교하였던 이전의 연구들에서 cisplatin이 반응율과 완전관해가 유의하게 높았기 때문입니다. 따라서 carboplatin은 cisplatin을 받지 못할 대상자(cisplatin-ineligible 또는 cisplatin-unfit population)에게만 추천됩니다. 문제는, 요로상피세포암 환자는 고령이며, 동반질환을 가진 경우가 많아 전체 환자의 50%이상에서 cisplatin의 대상이 아니라는 것이며, 그런 경우 carboplatin을 기반으로 한 항암제를 추천하게 되지만 효과가 만족스럽지 않습니다. 반응율은 약 40%로 높은 편이나, 무진행생존기간은 5.8개월, 전체생존기간 9.3개월로, 분명한 개선의 여지가 필요합니다. 게다가 carboplatin은 고령에서 특히 취약한 혈액학적 독성을 유발하므로 주의를 요합니다. Oxaliplatin은 백금계열 항암제로, cisplatin이나 carboplatin에 효과가 없는 암종에서도 효과가 입증되어 있고, carboplatin에 비하여 혈액학적 독성이 낮다고 알려져 있어서 cisplain을 사용하지 못하는 요로상피세포암 환자에서의 연구가 필요한 상황이었습니다.
Q. 연구의 목적은?
요로상피세포암에서 gemcitabine-oxaliplatin의 효과에 대한 2상 연구들이 있었지만, 소규모의 단일군 연구였습니다. 단일군 연구의 문제점은 다른 치료와의 효과를 비교하기 어렵다는 것입니다. 이에 본 연구에서는 cisplatin-ineligible환자에서 현재의 표준치료인 gemcitabine-carboplatin과 gemcitabine-oxaliplatin의 효과를 비교하는 것을 목적으로 하여 무작위 배정 2상 연구를 계획하였고, 1차 목표는 객관적 반응율로 하였습니다.
Q. 연구 방법?
본 연구는 제 2상 다기관 무작위배정 공개 임상시험이며, KCSGS GUGY 분과에서 논의되고 진행되었습니다. 국소진행성 또는 전이성 요로상피암 환자 중, 이전 항암치료를 받은 경험이 없으면서 Cisplatin 치료에 적합하지 않은 환자(ECOG PS 2, 사구체 여과율<60mL/min, 또는 NYHA 2-3등급의 심부전을 가진 자)를 대상으로 1차 치료로서 gemcitabine-oxaliplatin의 효과를 확인하기 위한 연구로 진행되었고, 1:1 무작위배정을 통해 gemcitabine-carboplatin (GCb, 현재의 표준치료)과 gemcitabine-oxaliplain(GEMOX, 임상시험치료)로 배정하여 투약하였습니다. 무작위배정은 참여기관, ECOG PS, 내장전이여부에 따라 층화하였습니다. 치료는 24주 (GCb 8주기, GEMOX 12주기)동안 투여되었습니다.
Q. 연구의 배경은?
진행성 요로상피세포암 (urothelial cancer)의 일차 표준요법은 백금기반 항암제이며, 백금제제 중에서도 cisplatin을 기반으로 하는 복합항암제가 추천됩니다. 백금제제에는 여러 약제가 있지만, cisplatin이 특별히 추천되는 이유는 cisplatin과 carboplatin을 비교하였던 이전의 연구들에서 cisplatin이 반응율과 완전관해가 유의하게 높았기 때문입니다. 따라서 carboplatin은 cisplatin을 받지 못할 대상자(cisplatin-ineligible 또는 cisplatin-unfit population)에게만 추천됩니다. 문제는, 요로상피세포암 환자는 고령이며, 동반질환을 가진 경우가 많아 전체 환자의 50%이상에서 cisplatin의 대상이 아니라는 것이며, 그런 경우 carboplatin을 기반으로 한 항암제를 추천하게 되지만 효과가 만족스럽지 않습니다. 반응율은 약 40%로 높은 편이나, 무진행생존기간은 5.8개월, 전체생존기간 9.3개월로, 분명한 개선의 여지가 필요합니다. 게다가 carboplatin은 고령에서 특히 취약한 혈액학적 독성을 유발하므로 주의를 요합니다. Oxaliplatin은 백금계열 항암제로, cisplatin이나 carboplatin에 효과가 없는 암종에서도 효과가 입증되어 있고, carboplatin에 비하여 혈액학적 독성이 낮다고 알려져 있어서 cisplain을 사용하지 못하는 요로상피세포암 환자에서의 연구가 필요한 상황이었습니다.
Q. 연구의 목적은?
요로상피세포암에서 gemcitabine-oxaliplatin의 효과에 대한 2상 연구들이 있었지만, 소규모의 단일군 연구였습니다. 단일군 연구의 문제점은 다른 치료와의 효과를 비교하기 어렵다는 것입니다. 이에 본 연구에서는 cisplatin-ineligible환자에서 현재의 표준치료인 gemcitabine-carboplatin과 gemcitabine-oxaliplatin의 효과를 비교하는 것을 목적으로 하여 무작위 배정 2상 연구를 계획하였고, 1차 목표는 객관적 반응율로 하였습니다.
Q. 연구 방법?
본 연구는 제 2상 다기관 무작위배정 공개 임상시험이며, KCSGS GUGY 분과에서 논의되고 진행되었습니다. 국소진행성 또는 전이성 요로상피암 환자 중, 이전 항암치료를 받은 경험이 없으면서 Cisplatin 치료에 적합하지 않은 환자(ECOG PS 2, 사구체 여과율<60mL/min, 또는 NYHA 2-3등급의 심부전을 가진 자)를 대상으로 1차 치료로서 gemcitabine-oxaliplatin의 효과를 확인하기 위한 연구로 진행되었고, 1:1 무작위배정을 통해 gemcitabine-carboplatin (GCb, 현재의 표준치료)과 gemcitabine-oxaliplain(GEMOX, 임상시험치료)로 배정하여 투약하였습니다. 무작위배정은 참여기관, ECOG PS, 내장전이여부에 따라 층화하였습니다. 치료는 24주 (GCb 8주기, GEMOX 12주기)동안 투여되었습니다.
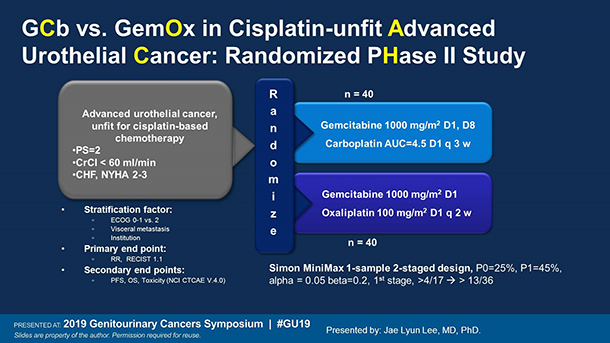
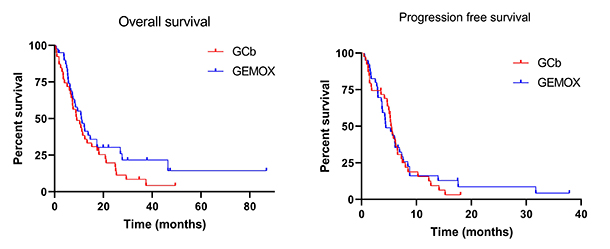
결과적으로, GEMOX는 GCb에 비하여 반응율과 생존기간이 수치상으로 더 높았으며, 흔한 부작용의 종류가 달랐습니다. 추가적인 분석에서, 신기능에 따라 용법에 따른 효과의 차이가 나는지 확인하기 위하여 사구체여과율에 따라 3군(사구체여과율<30 mL/min, 30-60, ≥60)으로 나누어 각 군에서의 반응율을 보았을 때, 30 mL/min 미만인 인구에서 GCb의 반응율은 0%(0/3)였던 것에 반하여 GEMOX의 반응율은 60%(3/5)였으며, 30-60에서는 GCb 48%(14/29)와 GEMOX 59%(17/29), 60이상에서는 GCb 71%(5/7), GEMOX 33.3%(2/6)으로, GCb는 신기능이 매우 낮은 군(CKD stage4-5)에서 효과가 낮지만 GEMOX는 효과가 유지된다는 인상을 받았습니다. 이는 지금까지는 알려져 있지 않았던 현상으로, 우연의 결과인지 실제 신기능과 효과가 연관이 있는 것인지 추가로 연구 중입니다. Q. 마지막으로 하고 싶은 말은? 요로상피세포암은 오랫동안 치료제의 발전이 없었으나, 최근 10년 사이 면역관문억제제, FGFR억제제, 항체약물결합체의 효과가 입증되어 매우 빠르게 발전 중입니다. 그럼에도 불구하고 항암치료는 전이성 요로상피세포암 환자는 물론이고, 수술로 완치가 가능한 비전이성 환자에 있어서도 여전히 가장 중요한 치료법입니다. Cisplatin-unfit환자는 진료현장에서 마주치는 요로상피암 환자군의 50%이상을 차지하는 중요한 환자군인데도 불구하고, 임상시험에 참여하기 어려운 취약한 대상자여서 임상시험이 많지 않고 따라서 높은 근거수준의 진료지침도 없는 상황입니다. 이러한 현실에서 한국에서 IIT로 연구를 진행하였다는 점에서 큰 의의가 있다고 자부하며, 한국의 연구자들이 비뇨기암 연구에서 두각을 나타낼 수 있는 기반이 되었다고 생각합니다. 마지막으로 본 연구를 계획하고, 진행하는데 도움을 주신 KCSG GUGY분과 모든 선생님들과, 연구에 참여해 주신 환자와 보호자분들께 진심으로 감사의 말씀을 올립니다. 제1저자 박인근 (가천대학교 길병원) 
■ KCSG BR15-10 Lancet Oncol. 2019 Dec;20(12):1750-1759 Palbociclib plus exemestane with gonadotropin-releasing hormone agonist versus capecitabine in premenopausal women with hormone receptor-positive, HER2-negative metastatic breast cancer (KCSG-BR15-10): a multicentre, open-label, randomised, phase 2 trial.  Q. 연구의 배경은?
ER+/HER2- 전이성 유방암에 대한 기존 치료법은 폐경 후 주로 발병하는 서양 환자를 대상으로 한 연구에 기반을 둔 터라 우리 현실과 차이가 있다. 우리나라의 경우 전이성 유방암 환자 절반이 50세 이하로 젊다. 치료 가이드라인과 대부분의 임상연구도 주로 폐경 후 여성을 대상으로 하여 이루어 지는 현실을 감안하여 폐경 전 많은 전이성 유방암 환자들에 표준요법으로 쓰여지고 있는 항암화학요법의 하나인 capecitabine을 대조군으로 하여 시행한 임상시험이다. 최근 ER+/HER2- 전이성 유방암의 현저한 치료효과를 보여주고 있는 CDK4/6 inhibitor의 하나인 palbociclib 과 호르몬 요법을 병합하여 시험군으로 하여 폐경 전 환자에 대한 치료 효과를 밝히고자 하였다.
Q. 연구의 목적은?
GnRH agonist인 leuprolide와 steroidal AI (Aromatase Inhibitor) 인 exemestane과 함께 CDK4/6 inhibitor인 palbocilcib 을 시험군으로 하여 표준요법으로 대조군인 capecitabine 과의 제2상 임상시험으로 PFS 의 우위가 있는 지를 보고자 한 연구이다.
Q. 연구 방법?
지난 2016년부터 2018년 사이 국내 14곳 의료기관에서 등록한 환자 189명을 대상으로 한 randomized phase 2, 2-arm의 전향적 임상연구로 KCSG의 유방암 분과에서 연구자 의뢰 임상시험으로 시행한 연구이다.
Q. 연구의 배경은?
ER+/HER2- 전이성 유방암에 대한 기존 치료법은 폐경 후 주로 발병하는 서양 환자를 대상으로 한 연구에 기반을 둔 터라 우리 현실과 차이가 있다. 우리나라의 경우 전이성 유방암 환자 절반이 50세 이하로 젊다. 치료 가이드라인과 대부분의 임상연구도 주로 폐경 후 여성을 대상으로 하여 이루어 지는 현실을 감안하여 폐경 전 많은 전이성 유방암 환자들에 표준요법으로 쓰여지고 있는 항암화학요법의 하나인 capecitabine을 대조군으로 하여 시행한 임상시험이다. 최근 ER+/HER2- 전이성 유방암의 현저한 치료효과를 보여주고 있는 CDK4/6 inhibitor의 하나인 palbociclib 과 호르몬 요법을 병합하여 시험군으로 하여 폐경 전 환자에 대한 치료 효과를 밝히고자 하였다.
Q. 연구의 목적은?
GnRH agonist인 leuprolide와 steroidal AI (Aromatase Inhibitor) 인 exemestane과 함께 CDK4/6 inhibitor인 palbocilcib 을 시험군으로 하여 표준요법으로 대조군인 capecitabine 과의 제2상 임상시험으로 PFS 의 우위가 있는 지를 보고자 한 연구이다.
Q. 연구 방법?
지난 2016년부터 2018년 사이 국내 14곳 의료기관에서 등록한 환자 189명을 대상으로 한 randomized phase 2, 2-arm의 전향적 임상연구로 KCSG의 유방암 분과에서 연구자 의뢰 임상시험으로 시행한 연구이다.
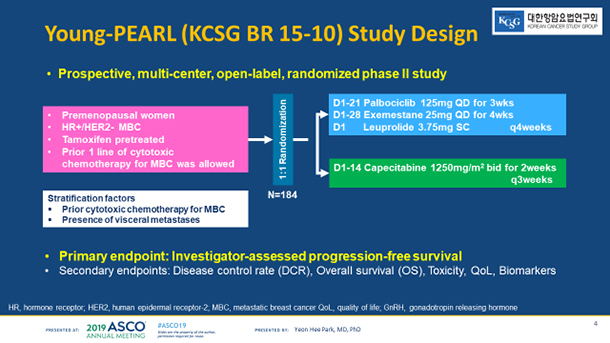
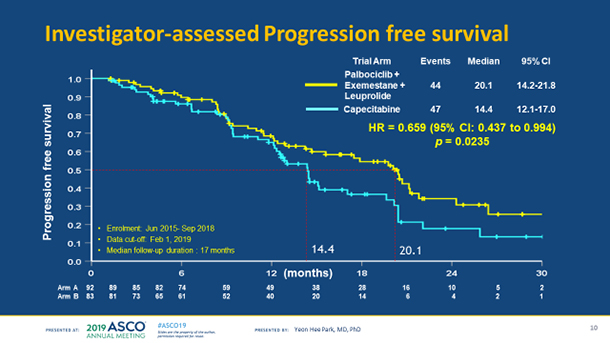
또한, 공익적 임상시험의 유방암 암정복 과제 중 세부과제로 진행되 바로 더욱 뜻 깊은 연구이다. 국내 다기관 임상시험을 성공적으로 유방암 분과에서 진행하여 그 성과를 ASCO에서 발표한 연구로 KCSG의 임상 연구의 한 성공적인 예로 연구에 물심양면으로 열과 성의로 참여하여 주신 유방암 분과 위원님들께 깊은 감사를 드리는 바이다. 제1저자 박연희 (삼성서울병원) 
|



