Q. 연구의 목적은?
70세 이상의 노인 전이성/재발성 위암 환자들을 대상으로 fluoropyrimidine/platinum의 2제 복합항암요법이 fluoropyrimidine 단독요법에 비하여 생존 기간의 연장 등 치료 측면에서 우월함을 확인하고, 내약성을 비교하는 것이 본 연구의 목적이었습니다.
Q.연구 방법?
본 연구는 국내 14개 기관이 참여한 다기관 3상 임상시험으로 시행되었습니다. 등록된 환자들을 1:1로 무작위 배정하여, 절반의 환자는 fluoropyrimidine/platinum의 2제 복합항암요법[FOLFOX (5-FU/Leucovorin/Oxaliplatin), CapOx (Capecitabine/Oxaliplatin) 혹은 S-1/Cisplatin]을 시행 받았고, 나머지 절반의 환자는 fluoropyrimidine 단독요법[FL (5-FU/Leucovorin), Capecitabine 혹은 S-1]을 시행 받았습니다. 복합요법에 배정된 환자들에서는 항암치료 첫 주기에는 약 75~80% 정도의 감량된 용량으로 항암치료를 시작한 후, 부작용 발생 정도에 따라 두번째 주기부터는 용량을 유지하거나 100%로 증량하는 방식으로 치료를 진행을 하였습니다. 본 연구의 primary endpoint는 overall survival (OS)이었고, secondary endpoint는 progression-free survival (PFS) 및 종양 반응률 등이 포함되었습니다.
Q. 연구 결과?
2014년 2월부터 환자 등록이 시작되었으며, 환자 등록이 쉽지 않아 2019년 1월까지 등록 기간이 연장되어 총 60개월에 걸쳐 111명의 전이성/재발성 노인 위암 환자들이 등록되었습니다. 노인 암 환자들을 대상으로 임상시험을 시행하다 보니 예상했던 대로 환자 등록이 쉽지 않아서, 원래 목표했던 등록 환자 숫자는 238명이었으나, 실제로는 약 절반 정도의 환자만 등록이 된 상태에서 본 연구는 종료되었습니다.
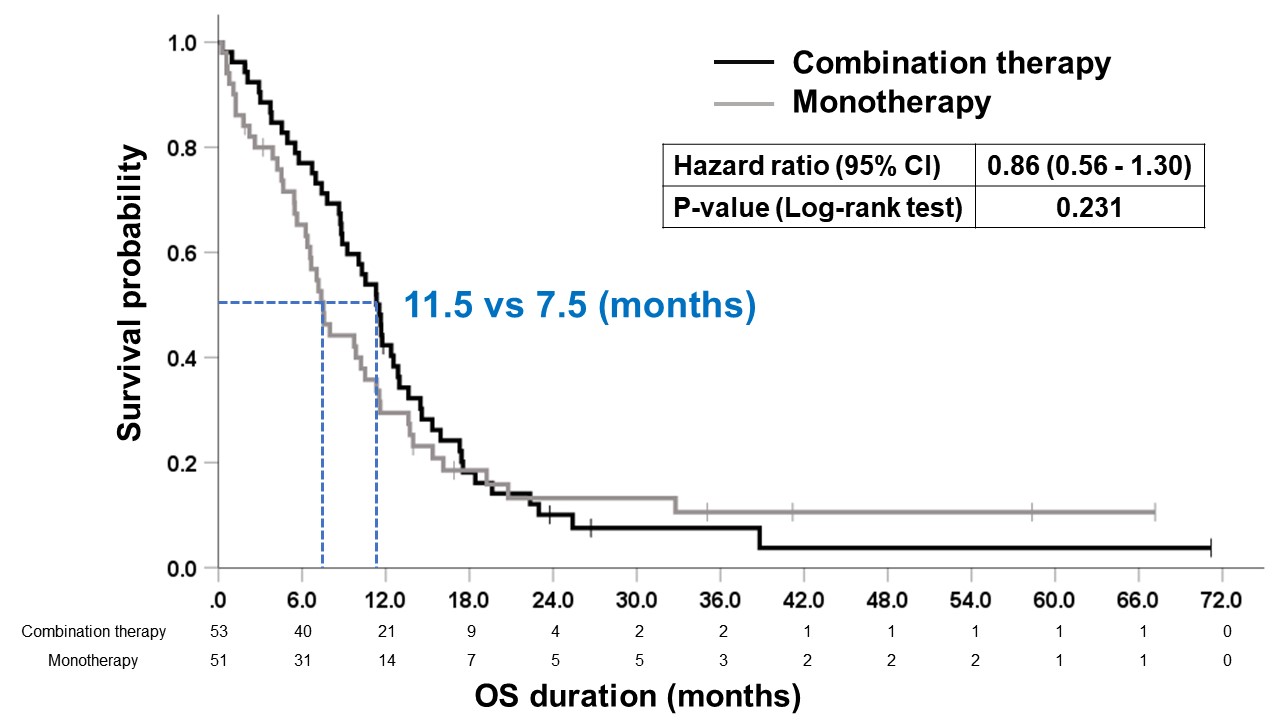
[그림1]
양군 사이의 OS을 비교하였을 때, 복합요법군과 단독요법군의 중앙 생존값은 각각 11.5개월 대 7.5개월로 4개월의 차이가 있었으나, 그 차이는 통계적으로 유의하지 않았습니다 [hazard ratio (HR), 0.86; 95% confidence interval (CI), 0.56?1.30; p=0.231; 그림 1]. 이 4개월의 OS의 차이는 임상적인 관점에서는 의미가 있어 보였지만 통계적으로는 유의하지 않았는데, 이는 목표한 연구대상자 등록이 달성되지 못하여 통계적인 파워가 충분치 못했던 것으로 판단되었습니다. 특히 환자들을 75세를 기준으로 하여 하위그룹 분석을 시행하였을 때, 75세 미만의 노인 환자들에서는 양군 사이의 OS의 차이가 더욱 명확해지는 경향성을 보였습니다 [OS의 중앙값 (복합요법 대 단독요법), 15.9개월 vs. 7.2개월; HR 0.53; 95% CI, 0.28?1.03; p=0.056].
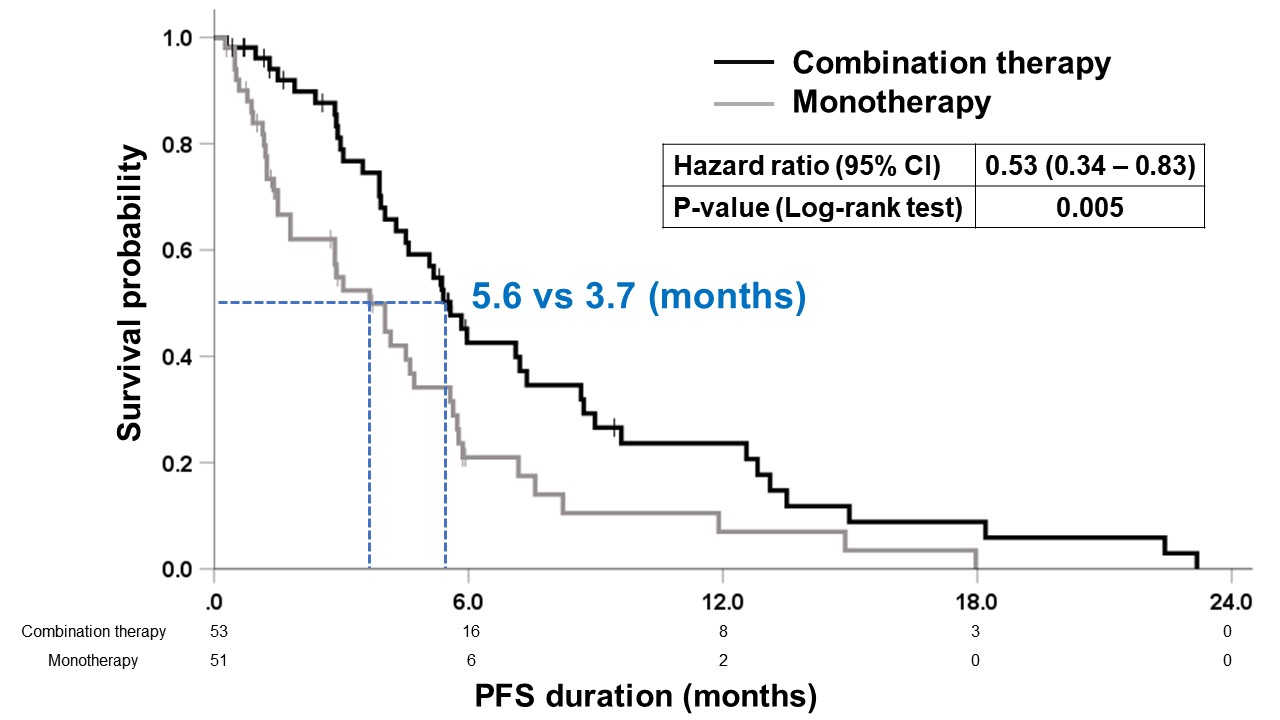
[그림2]
반면 secondary endpoint였던 양군 사이의 PFS을 비교하였을 때, 복합요법군과 단독요법군의 중앙 생존값은 각각 5.6개월 대 3.7개월로 통계적으로 유의한 차이가 확인되었습니다 [HR, 0.53; 95% CI, 0.34?0.83; p=0.005; 그림 2]. 치료와 관련된 부작용 발생 빈도를 비교하였을 때, 복합요법에서 단독요법에 비하여 전체적인 부작용 발생 빈도는 증가하였으니, grade 3 이상의 심한 부작용은 양군 사이에 큰 차이가 없었습니다.
Q. 마지막으로 하고 싶은 말은?
목표한 숫자의 환자 등록을 달성하지 못함으로 인해 본 연구의 primary endpoint를 입증하지 못하여 매우 아쉬웠습니다. 전이성/재발성 노인 위암 환자들에서 복합요법군과 단독요법군 사이의 OS의 차이를 통계적으로 입증하는 것에는 실패하였습니다만, 양군의 절대적 수치의 차이가 약 4개월이 됨을 확인되어 임상적으로는 유의해 보이는 수준임을 확인하였고, PFS의 차이는 양군 사이에 명확하게 확인되었습니다. 본 연구를 통하여 전신 상태가 양호한 전이성/재발성 노인 위암들, 특히 75세 미만의 환자들에서는 fluoropyrimidine/platinum 복합요법을 적극적으로 권할 수 있는 우리나라 자체의 근거는 어느 정도 마련을 했다고 생각합니다.
본 3상 임상시험의 디자인, 수행 및 마무리의 모든 과정에 함께 참여하면서 실전에서 많은 것을 배울 수 있었습니다. 본 과제는 암정복 과제로 시행이 되었는데, 총괄 책임자였던 서울의대/보라매병원의 최인실 교수님께서 정말 고생을 많이 하셨고, 큰 역할을 하셨습니다. 아울러 본 연구의 통계적 디자인과 분석에 큰 도움을 주셨던 남병호 박사님과 헤링스 회사의 담당자님들 및 조력해주신 KCSG 데이터센터 담당자님들께도 감사드립니다. 그리고 무엇보다도 본 연구에 참여하셨던 환자분들과 가족들, 그리고 많은 노력과 큰 도움을 주셨던 KCSG 산하 여러 기관의 동료 선생님들께도 큰 감사의 마음을 표합니다.

 회원검색
회원검색 통합검색
통합검색 교육신청
교육신청 연구검색
연구검색 데이터
데이터 TOP
TOP


