KCSG 소식

- 알림
- KCSG 소식
| 주요 연구성과 | 간행물 | 미디어 | 연구회동정 | KCSG 인사이트 | 뉴스레터 |
[KCSG HB23-04] J Hepatol. 2025 Sep 4:S0168-8278(25)02457-2.
- 작성자 관리자
- 등록일 2026-03-16
- 조회수 10
Multicenter phase II trial of lenvatinibin patients with advanced hepatocellular carcinoma after progression onfirst-line atezolizumab plus bevacizumab
저널: J Hepatol. 2025 Sep4:S0168-8278(25)02457-2. Online ahead of print.
제1저자 김형돈(서울아산병원)
Q. 연구의 배경은?
현재 전이성 또는 절제 불가능한 간세포암의 표준 1차 치료법은 면역항암제와혈관생성 억제제를 병용하는 '아테졸리주맙+베바시주맙(atezo-bev)' 요법입니다. 하지만 1차 치료에 실패한 이후 어떤 치료를 이어가야 하는지에 대해 세계적으로 확립된 표준 가이드라인이나 신뢰할 만한임상 데이터가 부족한 상황이었고, 특히 과거 1차 치료제로사용되던 렌바티닙이 1차 면역항암제 치료 실패 후에도 임상현장에서 사용되고 있었지만, 2차 요법으로 사용되는 렌바티닙의 전향적 근거가 부재한 상황이었습니다. 이에서울아산병원 유창훈 교수님의 주도로 연구가 진행되었고, 저는 연구 진행의 실무를 담당하며 연구를 진행하게되었고, KCGS의 도움으로 다기관 연구로 진행되었습니다.
Q. 연구의 목적은?
본 연구의 1차 목적은 1차치료제인 아테졸리주맙+베바시주맙 병용요법을 사용한 후 암이 진행된 간세포암 환자들을 대상으로, 2차 치료로서 렌바티닙 단독 요법의 유효성과 안전성을 평가하여 렌바티닙 사용의 전향적 근거를 마련하기 위함이었습니다.
Q. 연구 방법은?
이번 연구는 대한항암요법연구회(KCSG)의 지원을 받아 국내 13개 주요 대학병원에서 진행된 연구자 주도, 다기관, 단일군 2상 임상시험(KCSGHB23-04)으로, 약제 공급 및 연구에 대한 Eisai사의 지원이 있었습니다. 2023년 8월부터 2024년 5월까지 1차치료 후 암이 진행된 50명의 환자를 등록했습니다. 환자들은체중에 따라 렌바티닙 12mg 또는 8mg을 매일 경구 복용했으며, 연구의 1차 목표는 '무진행생존기간(PFS)'으로 설정하였으며, 그 외에도 전체 생존기간(OS), 객관적 반응률(ORR), 질병 조절률(DCR), 그리고 약제의 안전성을 분석했습니다.
Q. 연구 결과는?
연구 결과, 렌바티닙은 1차 치료에 실패한 환자들에게서 고무적인 효과를 보여주었습니다. 일차평가변수인 무진행 생존기간(중앙값)은 5.4개월로, 연구 설계 당시 목표로 했던 4.5개월을 상회하며 통계적 유의성을 확보하여, 본 연구는 1차 목표를 만족한 성공적인 연구였습니다. 또한 전체 생존기간 중앙값은 9.8개월을기록했습니다.
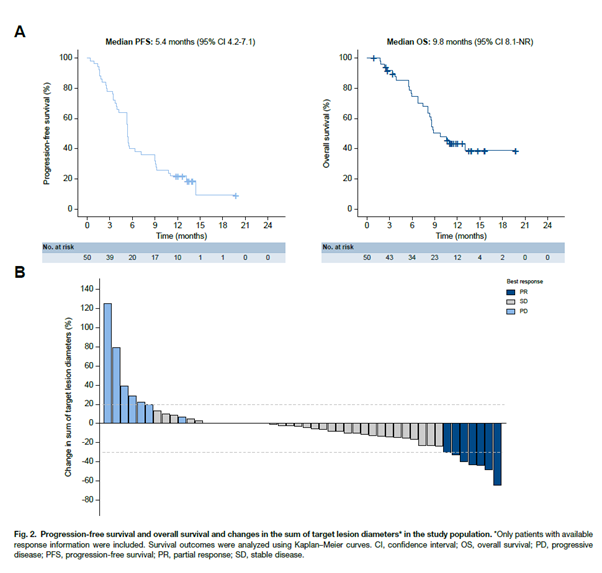
위의 그래프에서 확인할 수 있듯이, 대다수의 환자에서 종양 크기가 감소하거나 유지되는 양상을 보였으며, 실제환자의 82%에서 질병 조절 효과 가 나타났습니다. 객관적반응률은 14%였습니다. 부작용으로는 설사 (42%), 갑상선 기능 저하증 (32%) 등이 있었으나 관리 가능한수준이었습니다. 결론적으로 본 연구는 렌바티닙이 1차 면역항암제치료 후 선택할 수 있는 효과적인 2차 치료 대안임을 전향적 임상시험으로 세계 최초 증명했습니다.
Q. 마지막으로 하고 싶은 말은?
본 연구 결과와 함께 렌바티닙이 1차 면역항암제-기반 치료 이후의 요법으로 급여가 승인이 되어 더욱 의미 있게 생각합니다. atezo-bev이외에 다른 면역항암제 기반 치료도 널리 쓰일 것으로 예상되는데, 이 이후에 렌바티닙 사용이보험급여 적용이 결정되었지만, 마찬가지로 전향적인 근거는 없어 이에 대한 후속 연구도 계획 중입니다. 앞으로도 암환자분들께 도움이 되는 연구를 하는 연구자가 되도록 하겠습니다.
-
다음 글
다음글이 없습니다.
-
이전 글
[KCSG BR19-10] Lancet Reg Health West Pac. 2025 Jul 5:60:101622.
 회원검색
회원검색 통합검색
통합검색 교육신청
교육신청 연구검색
연구검색 데이터
데이터 TOP
TOP


